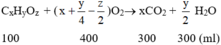Đốt cháy 10 ml khí Hidro trong 10 ml khí Oxi. Thể tích chất khí thu được sau PƯ là bao nhiêu? (Biết các chất khí đo ở điều kiện to và áp suất, nước ở trạng thái hơi.)

Những câu hỏi liên quan
Đốt cháy 10
c
m
3
khí hidro trong 10
c
m
3
khí oxi. Thể tích chất khí còn lại sau phản ứng: A. 5
c
m
3
hidro B. 10
c
m
3
hidro C. Chỉ có 10
c
m
3
hơi nước D. 5
c
m
3...
Đọc tiếp
Đốt cháy 10 c m 3 khí hidro trong 10 c m 3 khí oxi. Thể tích chất khí còn lại sau phản ứng:
A. 5 c m 3 hidro B. 10 c m 3 hidro
C. Chỉ có 10 c m 3 hơi nước D. 5 c m 3 oxi
Tìm câu trả lời đúng, biết các thể tích khí đo cùng ở 100 0 C và áp suất khí quyển.
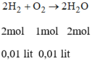
* Chú ý: cùng đktc: tỉ lệ số mol = tỉ lệ thể tích
Tỉ số mol của H 2 và O 2 :
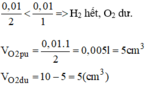
Chọn D
Đúng 0
Bình luận (0)
Đốt cháy 200 ml hơi một hợp chất hữu cơ X chứa C, H, O trong 900 ml O2, thể tích hỗn hợp khí thu được là 1,3 lít. Sau khi ngưng tụ hơi nước chỉ còn 700 ml. Tiếp theo cho qua dung dịch KOH dư chỉ còn 100 ml khí bay ra. Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. CTPT của Y là A. C3H8O2 B. C3H6O C. C3H6O2 D. C3H8O
Đọc tiếp
Đốt cháy 200 ml hơi một hợp chất hữu cơ X chứa C, H, O trong 900 ml O2, thể tích hỗn hợp khí thu được là 1,3 lít. Sau khi ngưng tụ hơi nước chỉ còn 700 ml. Tiếp theo cho qua dung dịch KOH dư chỉ còn 100 ml khí bay ra. Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. CTPT của Y là
A. C3H8O2
B. C3H6O
C. C3H6O2
D. C3H8O
Đốt cháy 100 ml hơi một hợp chất hữu cơ X (chứa C, H, O) trong 450 ml
O
2
, thu được 650 ml hỗn hợp khí và hơi. Sau khi ngưng tụ hơi nước chỉ còn 350 ml. Tiếp theo cho qua dung dịch KOH dư chỉ còn 50 ml khí bay ra. Các thể tích khí đo ở cùng điều kiện, nhiệt độ, áp suất. Công thức phân tử của X là A.
C
3
H
8
O
2...
Đọc tiếp
Đốt cháy 100 ml hơi một hợp chất hữu cơ X (chứa C, H, O) trong 450 ml O 2 , thu được 650 ml hỗn hợp khí và hơi. Sau khi ngưng tụ hơi nước chỉ còn 350 ml. Tiếp theo cho qua dung dịch KOH dư chỉ còn 50 ml khí bay ra. Các thể tích khí đo ở cùng điều kiện, nhiệt độ, áp suất. Công thức phân tử của X là
A. C 3 H 8 O 2
B. C 3 H 6 O
C. C 4 H 8 O
D. C 3 H 6 O 2
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 50 ml khí O2, thu được hỗn hợp Y gồm khí CO2 và hơi H2O có tỉ lệ thể tích tương ứng là 5 : 4. Ngưng tụ toàn bộ hơi H2O trong Y, thấy còn lại 50 mL khí. Biết các thể tích khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất. Phân tử khối của X là A. 86 B. 100 C. 132 D. 118
Đọc tiếp
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 50 ml khí O2, thu được hỗn hợp Y gồm khí CO2 và hơi H2O có tỉ lệ thể tích tương ứng là 5 : 4. Ngưng tụ toàn bộ hơi H2O trong Y, thấy còn lại 50 mL khí. Biết các thể tích khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất. Phân tử khối của X là
A. 86
B. 100
C. 132
D. 118
Chọn đáp án C
50 mL khí không bị ngưng tụ là C O 2 ; tỉ lệ n H 2 O : n C O 2 = 4 : 5
→ có 40 mL H 2 O
các khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất → chọn điều kiện V = 10 mL ⇄ 1 mol.
Ta có: đốt 1 mol este X cần 5 m o l O 2 → t 0 5 m o l C O 2 + 4 m o l H 2 O
BTNT oxi có trong X: n O = 4
→ số O = 4 : 1 = 4.
Lại có số C = 5 : 1 = 5 và số H = 4 × 2 : 1 = 8
→ CTPT của X là C 5 H 8 O 4
Tính được MX = 132
Đúng 0
Bình luận (0)
Đốt cháy hết 0,2 ml hơi của hợp chất (X) cần 0,06 ml khí oxi , thu được 0,4 ml CO2 và 0,06 ml hơi nước . Các thể tích khí và hơi đo cùng nhiệt độ áp xuất.Công thức phân tử của hợp chất (X) là.
Để xác định công thức phân tử của hợp chất (X), ta cần phân tích tỷ lệ thể tích các chất tham gia và sản phẩm của phản ứng cháy.
Theo thông tin trong đề bài, để đốt cháy hết 0,2 ml hơi của hợp chất (X), cần 0,06 ml khí oxi. Sản phẩm của phản ứng cháy là 0,4 ml CO2 và 0,06 ml hơi nước.
Ta biết rằng phản ứng cháy của hợp chất (X) có thể được biểu diễn bằng phương trình:
CₓHₓ + yO₂ → zCO₂ + wH₂O
Từ đó, ta có thể lập các phương trình cân bằng thể tích:
0,2 ml hơi (X) → 0,4 ml CO₂ 0,06 ml O₂ → 0,4 ml CO₂
Vì tỷ lệ giữa hơi (X) và O₂ là 1:0,3 (0,2 ml / 0,06 ml), và tỷ lệ giữa CO₂ và O₂ là 0,4:0,06 (0,4 ml / 0,06 ml), nên ta có thể suy ra tỷ lệ giữa hợp chất (X) và CO₂ là 1:0,75 (1:0,3 * 0,4:0,06).
Nếu ta giả sử số mol của hợp chất (X) là a, số mol của CO₂ là b, ta có thể viết lại tỷ lệ trên dưới dạng số mol:
a : 1 b : 0,75
Vì CO₂ có 1 mol cacbon (C) và 2 mol oxi (O₂) trong phân tử, nên số mol cacbon (C) trong hợp chất (X) cũng là b.
Vậy, công thức phân tử của hợp chất (X) là CbHb.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 50 ml hỗn hợp khí X gồm trimetylamin và hai hiđrocacbon đồng đẳng kế tiếp bằng một lượng oxi vừa đủ, thu được 375 ml hỗn hợp Y gồm khí và hơi. Dẫn toàn bộ Y đi qua dung dịch H2SO4 đặc (dư), thể tích khí còn lại là 175 ml. Các thể tích khí và hơi đo ở cùng điều kiện về nhiệt độ và áp suất. Hai hiđrocacbon đó là A. C2H6 và C3H8. B. C2H4 và C3H6. C. C3H6 và C4H8. D. C3H8 và C4H10.
Đọc tiếp
Đốt cháy hoàn toàn 50 ml hỗn hợp khí X gồm trimetylamin và hai hiđrocacbon đồng đẳng kế tiếp bằng một lượng oxi vừa đủ, thu được 375 ml hỗn hợp Y gồm khí và hơi. Dẫn toàn bộ Y đi qua dung dịch H2SO4 đặc (dư), thể tích khí còn lại là 175 ml. Các thể tích khí và hơi đo ở cùng điều kiện về nhiệt độ và áp suất. Hai hiđrocacbon đó là
A. C2H6 và C3H8.
B. C2H4 và C3H6.
C. C3H6 và C4H8.
D. C3H8 và C4H10.
Đáp án C
Trong cùng điều kiện nhiệt độ và áp suất thì tỉ lệ thể tích chính là tỉ lệ số mol.
Luôn có VH2O = 550- 250 = 300 ml , VCO2 + V N2 = 250 ml
Nếu hỗn hợp là hidrocacbon no (ankan)→ Vankan + Vamin = VH2O - VCO2 - VN2 = 50 < 100 ml ( Loại0
Nếu hỗn hợp là anken → Vanken= VH2O -VCO2 - VN2 = 50 ml → Vamin = 50 ml → VN2= 25ml
→ 50. 2+ 50.n = 250-25 → n = 2,5 → hai anken là C2H4 và C3H6.
Đáp án C.
Đúng 0
Bình luận (0)
Đốt cháy hết 0,2 ml hơi của hợp chất (X) cần 0,06 ml khí oxi , thu được 0,4 ml CO2 và 0,06 ml hơi nước . Các thể tích khí và hơi đo cùng nhiệt độ áp xuất.Công thức phân tử của hợp chất (X) là.
Các bạn giúp mh với , mh cảm ơn
Để tìm công thức phân tử của hợp chất (X), ta cần phân tích các thể tích khí và hơi mà ta thu được sau khi đốt cháy hợp chất (X).
Theo đề bài, khi đốt cháy hết 0,2 ml hơi của hợp chất (X), ta thu được 0,4 ml CO2 và 0,06 ml hơi nước. Đồng thời, ta cần 0,06 ml khí oxi để đốt cháy hết hợp chất (X).
Ta biết rằng trong quá trình đốt cháy, hợp chất (X) phản ứng với khí oxi (O2) và tạo ra CO2 và hơi nước. Vì vậy, ta có thể viết phương trình phản ứng như sau:
CnHmOx + O2 -> CO2 + H2O
Trong phương trình trên, CnHmOx là công thức phân tử của hợp chất (X), n, m, x lần lượt là số nguyên dương tương ứng với số nguyên mol của cacbon (C), hidro (H) và oxi (O) trong công thức phân tử.
Từ các thể tích mà ta thu được sau phản ứng, ta có thể xác định tỉ lệ giữa số mol của CO2 và H2O. Trong trường hợp này, tỉ lệ thể tích giữa CO2 và H2O là 0,4 ml : 0,06 ml = 6,67 : 1.
Từ đó, ta có thể xác định tỉ lệ số mol giữa CO2 và H2O, và từ đó xác định tỉ lệ số mol giữa cacbon và hidro trong công thức phân tử của hợp chất (X).
Tuy nhiên, trong đề bài không cung cấp đủ thông tin về các giá trị số mol của CO2 và H2O, cũng như số mol của hợp chất (X). Vì vậy, không thể xác định được công thức phân tử của hợp chất (X).
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 45 ml O2, sau phản ứng thu được hỗn hợp khí CO2 và hơi nước có tỉ lệ thể tích là 4 : 3. Ngưng tụ sản phẩm cháy thì thể tích giảm đi 30 ml. Biết các thể tích đo ở cùng điều kiện. Công thức của este X là A. C4H6O2 B. C4H6O4 C. C4H8O2 D. C8H6O4
Đọc tiếp
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 45 ml O2, sau phản ứng thu được hỗn hợp khí CO2 và hơi nước có tỉ lệ thể tích là 4 : 3. Ngưng tụ sản phẩm cháy thì thể tích giảm đi 30 ml. Biết các thể tích đo ở cùng điều kiện. Công thức của este X là
A. C4H6O2
B. C4H6O4
C. C4H8O2
D. C8H6O4
Chọn đáp án A
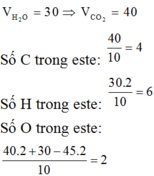
Vậy, công thức este là C 4 H 6 O 2
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 45 ml O2, sau phản ứng thu được hỗn hợp khí CO2 và hơi nước có tỉ lệ thể tích là 4 : 3. Ngưng tụ sản phẩm cháy thì thể tích giảm đi 30 ml. Biết các thể tích đo ở cùng điều kiện. Công thức của este X là A. C4H6O2 B. C4H6O4 C. C4H8O2 D. C8H6O4
Đọc tiếp
Đốt cháy hoàn toàn 10 ml hơi một este X cần vừa đủ 45 ml O2, sau phản ứng thu được hỗn hợp khí CO2 và hơi nước có tỉ lệ thể tích là 4 : 3. Ngưng tụ sản phẩm cháy thì thể tích giảm đi 30 ml. Biết các thể tích đo ở cùng điều kiện. Công thức của este X là
A. C4H6O2
B. C4H6O4
C. C4H8O2
D. C8H6O4
Đáp án: A
V H 2 O = 30 ⇒ V C O 2 = 40
Số C trong este:
40
10
=
4
Số H trong este:
30
.
2
10
=
6
Số O trong este:
40
.
2
+
30
-
45
.
2
10
=
2
Vậy, công thức este là C4H6O2
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 20 ml hơi hợp chất hữu cơ X (chỉ gồm C, H, O) cần vừa đủ 110 ml khí O2, thu được 160 ml hỗn hợp Y gồm khí và hơi. Dẫn Y qua dung dịch H2SO4 đặc (dư), còn lại 80 ml khí Z. Biết các thể tích khí và hơi đo ở cùng điều kiện. Công thức phân tử của X là: A. C4H10O. B. C4H8O. C. C3H8O. D. C4H8O2.
Đọc tiếp
Đốt cháy hoàn toàn 20 ml hơi hợp chất hữu cơ X (chỉ gồm C, H, O) cần vừa đủ 110 ml khí O2, thu được 160 ml hỗn hợp Y gồm khí và hơi. Dẫn Y qua dung dịch H2SO4 đặc (dư), còn lại 80 ml khí Z. Biết các thể tích khí và hơi đo ở cùng điều kiện. Công thức phân tử của X là:
A. C4H10O.
B. C4H8O.
C. C3H8O.
D. C4H8O2.
Ta có
![]()

=> Loại A và C
C4H8Ox + 12 - x 2 O2 → 4CO2 + 4H2O
20 ml 110 ml
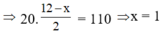
=> X là C4H8O
=> Chọn B.
Đúng 0
Bình luận (0)